Autores
Gonzalez Alejandro, Artazcoz Santiago, Quiñones Agustín, Jurío Gastón, Toziano Mariano, Benvenuto Ricardo.
Lugar de realización
Hospital Naval Pedro Mallo, Sanatorio de la Trinidad Mitre,
Introducción
El desarrollo de la Neuropelveología (1) ha provocado una revolución en los conocimientos anatómicos y funcionales de la pelvis: identificación de nervios y plexos pelvianos mediante la Técnica de Neuronavegación (LANN: Laparoscopic Neuro-Navigation) (2), estudio y tratamiento de las patologías de la pelvis y la columna vertebral que afectan los nervios y plexos pelvianos, diagnósticos clínicos-neurológicos y procedimientos laparoscópicos neuro-funcionales: cirugía con preservación nerviosa (nerve sparing), cirugía de descompresión nerviosa, neurolisis, neuroestimulación externa o la novedosa Técnica LION (Laparoscopic Implantation of Neuroprotesis) para neuroestimulación directa de los nervios pelvianos por vía anterior (3,4).
Con el aumento del número de los casos tratados y con el estudio en profundidad de las alternativas diagnósticas y terapéuticas del dolor pelviano crónico surgen nuevos síndromes y nuevos desafíos. El dolor pelviano neuropático por atrapamiento neurovascular y muscular es uno de ellos (5).
Habitualmente negado o ignorado, se presenta en pacientes con dolor pelviano crónico incoercible e invalidante con gran afectación de su calidad de vida, con dolores similares a descargas eléctricas en las dermatomas afectadas, con o sin antecedentes y que reciben todo tipo de tratamientos médicos, e incluso quirúrgicos, con respuesta fallida.
El dolor neuropático es aquel que persiste después de la curación de la enfermedad o de daño titular inducido por trauma, es un dolor aberrante, desproporcionado, con una falta total de relación causal entre lesión titular y dolor. El síndrome de atrapamiento nervioso o compresión neuropática se produce por atrapamientos de las porciones intrapélvicas de los nervios somáticos y/o autonómicos que producirán síntomas en la dermatoma afectada o viscerales y/o vegetativos.
Las causas más frecuentes son la fibrosis de los tejidos primaria o secundaria a procesos inflamatorios, los traumas quirúrgicos (uso de retractores de pared, episiotomías, reparaciones con mallas, etc), patologías como la endometriosis profunda, atrapamientos vasculares por dilatación y/o malformación de vasos (Foto 1) y atrapamientos musculares (Foto 2) y/o ligamentarios (Foto 3)
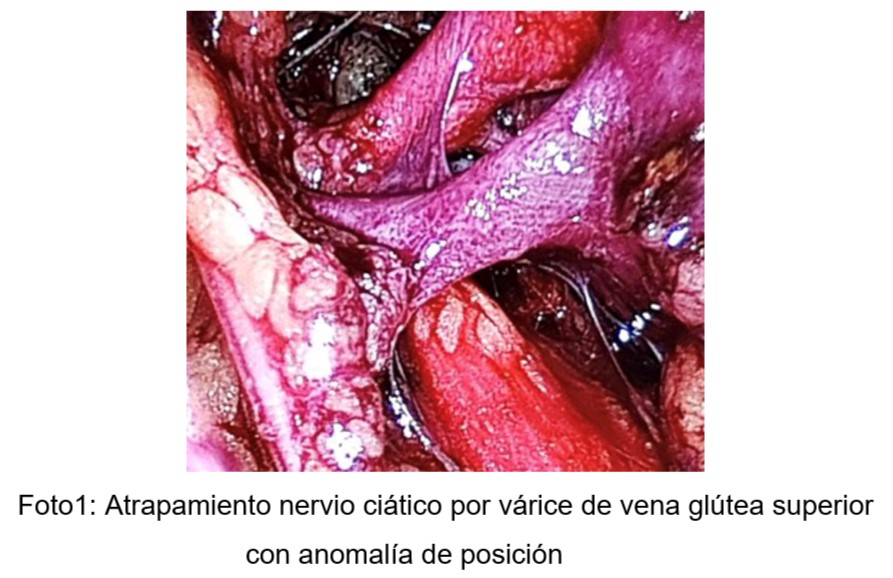
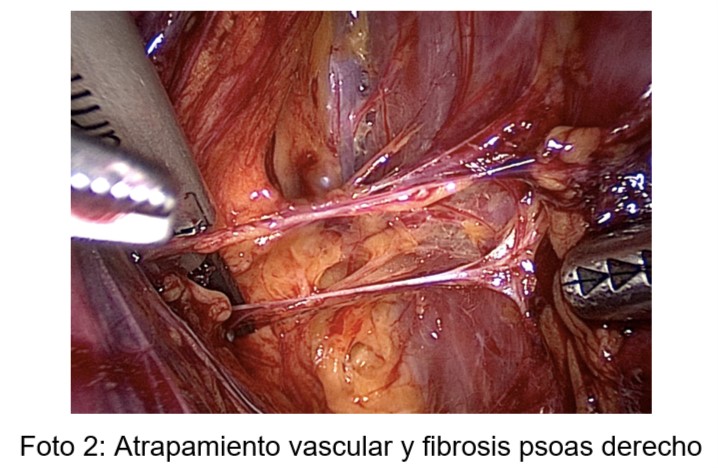
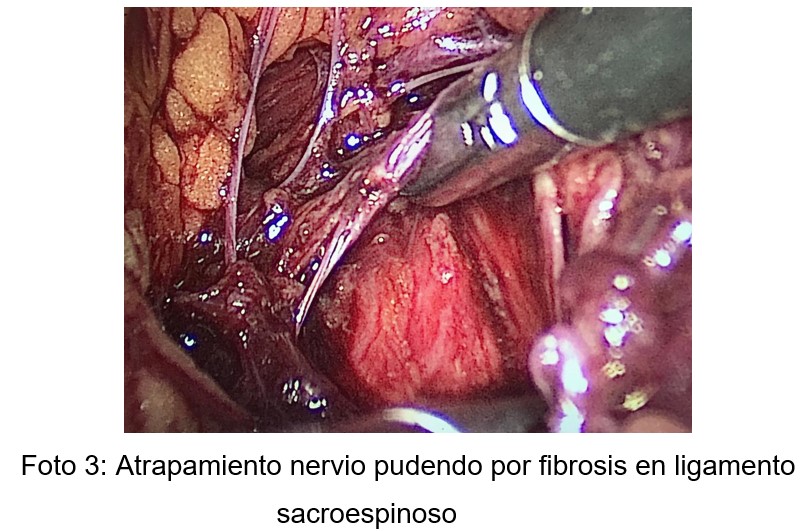
La causa más frecuente de dolor pelviano por contractura del psoas ilíaco es la fibrosis perimuscular que suele comprometer también el nervio genitofemoral con afectación somática y limitación de los movimientos (Foto 4). Generalmente se acompaña de aumento de la trama vascular con varices de los vasos del músculo obturador y otros vasos anómalos.
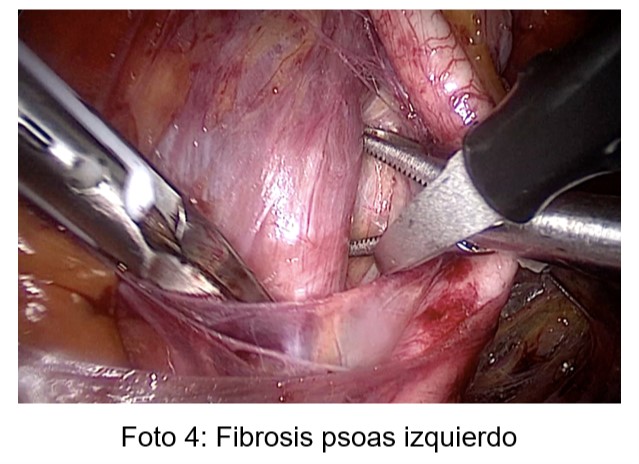
El primer antecedente de dolor pelviano neuropático por atrapamiento fue descripto por Amarenco G en 1987 sobre 15 casos de neuralgia perineal por compresión de nervio pudendo en el canal de Alcock, tratados con infiltraciones con corticoides guiado por tomografia axial computada (TAC) informando un resultado satisfactorio en 9 de las 15 pacientes (6,7).
No obstante, luego de la descripción de Amarenco, hubo un largo tiempo sin nuevos aportes trascendentales hasta la irrupción de las técnicas de nerve sparing primero, sobre todo en histerectomía radical por carcinoma de cuello uterino y endometriosis profunda (8,9,10) y fundamentalmente el desarrollo de la Neuropelveología después (11,12,13).
Es así como comienzan a surgir nuevos trabajos sobre neuroanatomía pelviana con distintos enfoques. Lemos N. describe la anatomía laparoscópica de los nervios intrapelvianos con sus causas más frecuentes de atrapamiento y los divide en 4 grupos principales (5):
- Ilio-hipogástrico, ilio-inguinal y genito-femoral
- Nervio femoral
- Nervios del Espacio-canal obturador
- Obturador
- Tronco Lumbosacro
- Ciático
- Pudendo
- Nervios de S3-S4 (fibras posteriores del Elevador del ano)
- Nervios presacros y del espacio pararectal
- Plexo hipogástrico superior-nervio hipogástrico-plexo hipogástrico inferior
- Plexo sacro-nervios esplácnicos
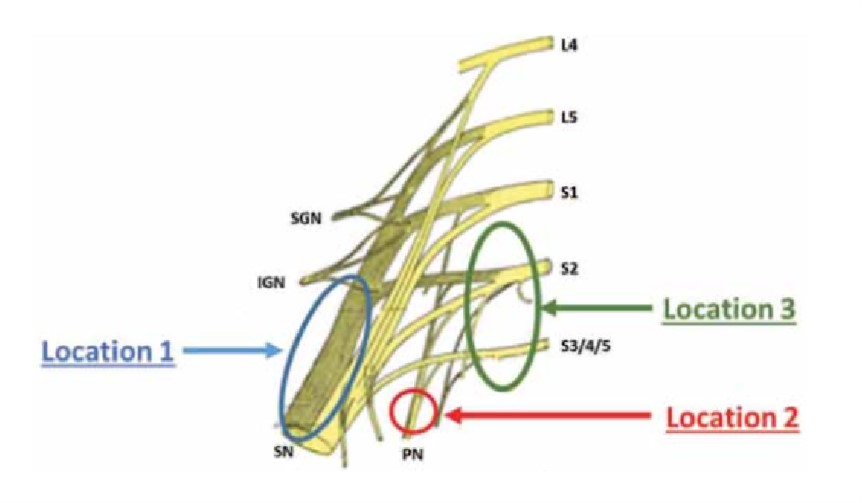
Y Possover M, en 2015, describe los 3 hallazgos anatómicos más frecuentes en las neuralgias pelvianas por atrapamiento neuro-vascular (14):
- Localización 1: Compresión porción distal tronco lumbosacro
- Localización 2: Compresión del nervio pudendo (Sind canal de Alcock)
- Localización 3: Compresión de raíces sacras (S2-S4)
El diagnóstico de estos síndromes se basa en 5 pasos: confección de una adecuada historia clínica, un examen físico completo basado en conceptos clínicos-neurológicos, la realización de una ecografía transvaginal (ETV) (o transrectal), Resonancia Magnética Nuclear (RMN) con secuencia neurográfica y eventualmente una laparoscopía para confirmar diagnóstico y efectuar el tratamiento en el mismo acto.
El dolor provocado por el atrapamiento suele ser severo e incapacitante, por afección del plexo lumbar y/o sacro, con valores altos en la escala visual analógica (VAS) habitualmente entre 8 y 10, de tipo somático, caracterizado por su ubicación específica fácilmente identificable por la paciente, falta de síntomas vegetativos, presencia de alodinia o descargas eléctricas, de localización superficial en la piel y con irradiación en áreas genito-anales o extremidades inferiores.
Los síntomas principales de irritación de nervios somáticos incluyen: ciatalgia asociada con síntomas urinarios (urgencia,frecuencia,disuria) sin causa ortopédica (columna sana), dolor glúteo asociado dolor perineal, vaginal o peneano, dolor pudendo parcial o completo, vulvodinia, coccigodinia, disuria y/o dolor en la eyaculación, síntomas urinarios refractarios, y dolor pelviano y perineal refractario.
Cuando la respuesta al tratamiento médico es insatisfactoria y las terapias adyuvantes fallan, el tratamiento quirúrgico laparoscópico está indicado. Las opciones terapéuticas incluyen las liberaciones de las zonas fibróticas, la erradicación de la enfermedad de base, la sección de ligamentos afectados, la descompresión nerviosa, la neurolisis, la resección con o sin reconstrucción nerviosa y por último la neuromodulación externa o el procedimiento LION, que consiste en la colocación laparoscópica de un neuroestimulador (15) con el objetivo de modular e interferir la trasmisión nerviosa del dolor.
A continuación se presentará la primera serie de casos del país sobre tratamiento quirúrgico de descompresión laparoscópica en pacientes con dolor pelviano neuropático por atrapamiento neurovascular y muscular.
Propósito de la investigación
Hipótesis nula (H0): La cirugía de descompresión neuro-vascular somática y muscular no es eficaz para el tratamiento quirúrgico del dolor neuropático.
Hipótesis alternativa (H1): La cirugía de descompresión neuro-vascular somática y muscular es eficaz para el tratamiento quirúrgico del dolor neuropático y lo mejora de manera estadísticamente significativa.
Objetivos
Objetivo general
- Demostrar la eficacia de la cirugía de descompresión laparoscópica en pacientes con dolor pelviano neuropático severo por atrapamiento neuro-vascular somático y muscular.
Objetivos específicos
- Presentar las distintas técnicas y resultados terapéuticos.
- Demostrar su utilidad en pacientes con tratamientos médicos fallidos.
Material y métodos
Estudio observacional descriptivo retrospectivo cuasiexperimental sobre 28 pacientes asistidas e intervenidas en las Secciones de Endoscopía Ginecológica del Hospital Naval Buenos Aires y en el Sanatorio de la Trinidad Mitre en el período comprendido entre Septiembre de 2017 y Marzo de 2019.
Criterios de inclusión
Pacientes de cualquier edad con dolor pelviano crónico de tipo neuropático con sospecha de atrapamiento nervioso somático y/o muscular con respuesta fallida al tratamiento médico y/o terapias adyuvantes.
A todas las pacientes se les realizó:
- Historia clínica detallada y estructurada a tal fin (Anexos-Hoja 1) excepto ante sospecha de neuralgia del pudendo donde se utilizó otra historia clínica diseñada de acuerdo a criterios internacionales conocidos como Criterio de Nantes (Anexos-Hoja 2) (16).
- Examen físico neuropelveológico completo con evaluación de vías y nervios implicados en la génesis del dolor, y tacto vaginal para evaluar puntos gatillos y estado de ligamentos uterosacros.
- Ecografía transvaginal
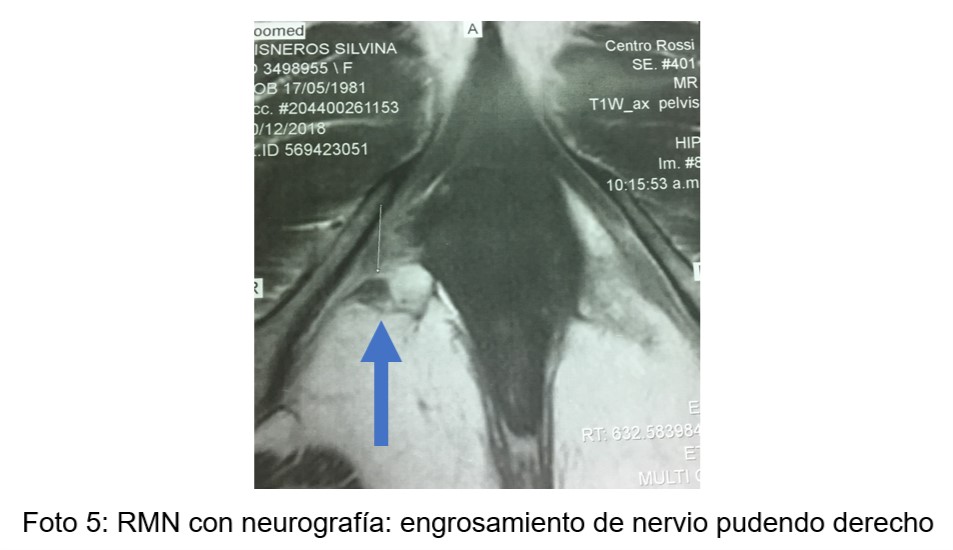
- RMN de piso pelviano con secuencia neurográfica sin contraste (Foto 5)
- Laparoscopía diagnóstica-terapéutica
Para la evaluación del dolor se utilizó la escala visual analógica (VAS) (17,18) considerando Dolor leve £3, dolor moderado entre 4 y 7 y dolor severo ³8.
Respecto a criterios de curación, mejoramiento o no, se consideró curación a la presencia de un VAS postoperatorio de 0-1, mejoramiento a todo descenso en la escala VAS que puede ser mayor o menor al 50% y sin cambios a la persistencia de un VAS de 8 a 10.
La RMN fue realizada siempre por el mismo operador con un resonador Philipsâ Ingenia 1.5 T con sistema MR avanzado.
Todas las laparoscopías fueron realizadas por el mismo cirujano y se utilizó una torre de alta definición full HD Storzâ modelo Image 1 Pure con instrumental de la misma marca. Se utilizaron dos tipos de energía: bipolar con pinza ROBIâ de agarre y coagulación y ultrasonido con bisturí armónico.
Las cirugías laparoscópicas se realizaron de manera sistemática con exploración y eventual tratamiento de los segmentos nerviosos y/o ligamentos y/o músculos afectados.
Se utilizaron 4 vías, con la siguiente disposición: umbilical, hipogastrio y ambas fosas ilíacas, con la paciente en posición de Trendelemburg extremo, a 45°.
Los nervios obturador, ciático y pudendo se abordaron en el espacio comprendido entre la cara medial del músculo psoas y los vasos ilíacos, primero el nervio obturador, luego en profundidad el tronco lumbosacro con el nervio ciático, y finalmente, sólo de ser necesario, el nervio pudendo hasta su entrada en el canal de Alcock con eventual sección del ligamento sacroespinoso.
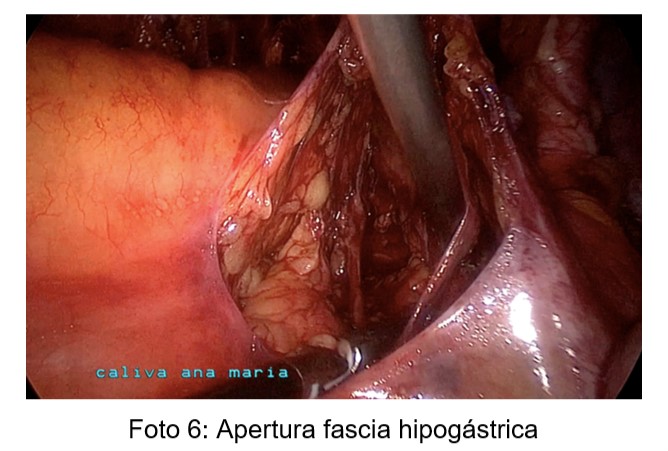
El plexo sacral se disecó mediante la apertura de las fascias hipogástricas (Foto 6) y sacral, en el espacio pararectal profundo, y hasta visualizar las raíces sacras y los nervios esplácnicos, según técnica descripta por Possover (2,5).
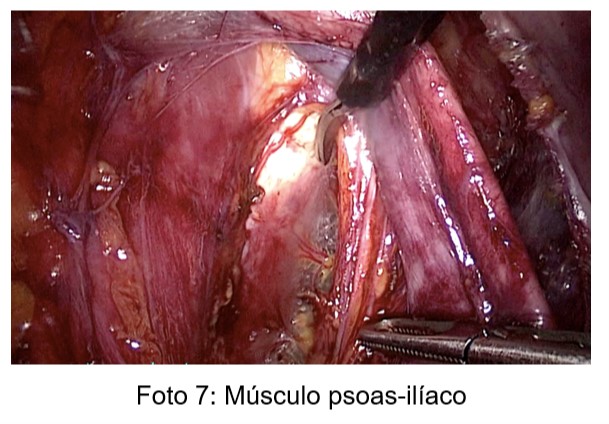
El acceso al músculo psoas y plexo lumbar también se realizó de manera reglada sistemática: se inicia con la desperitonización lateral entre el ligamento redondo y el ligamento infundibulopélvico hasta individualizar el nervio genitofemoral y el tendón del músculo psoas, cuyas ubicaciones pueden variar por la misma fibrosis. Luego se procede a la apertura de la fascia y liberación muy cuidadosa del fascículo muscular de manera que recupere la movilidad. Medialmente se lo separa de los vasos ilíacos hasta la identificación del nervio obturador, y de acuerdo a la fibrosis y los vasos anómalos es conveniente llegar a visualizar la inserción del fascículo ilíaco sobre el hueso de mismo nombre (Foto 7). Lateralmente debe disecarse hasta la visualización del nervio femoral. Ambos nervios constituyen reparos anatómicos pero no deben manipularse si no es necesario para evitar dolores neuropáticos nuevos.
Externo al nervio femoral se accede el resto del plexo lumbar: ilio-hipogástrico, ilio-inguinal y femoro cutáneo lateral.
La cirugía realizada fue la descompresión del segmento nervioso y/o muscular afectado, de acuerdo a la causa que lo provoque: ante la presencia de fibrosis se realizó la resección del tejido con el aislamiento y liberación del nervio; ante la presencia de malformaciones y/o dilataciones varicosas, la coagulación con energía bipolar de las mismas y la sección con bisturí armónico; y ante la presencia de endometriosis, el tratamiento completo de la enfermedad con técnica de nerve-sparing (preservación nerviosa). Ante la presencia de un atrapamiento de raíces sacras por fibras aberrantes del músculo piriforme, se realizó la liberación de la raíz afectada mediante la sección de las fibras musculares con bisturí armónico. En los casos que presentaban adenomiosis y/o miomatosis uterina sintomática se realizó también la histerectomía total laparoscópica.
En caso de existir fibrosis sobre el nervio genito-femoral con alteración anatómica y síntomas de compresión, debe liberarse en toda su extensión hasta la división en sus dos ramas: genital (medial, entrando por el canal inguinal) y femoral (lateral, pasando por debajo del ligamento inguinal). De ser necesario, se procederá a la liberación completa del plexo lumbar sensitivo (L1,L2)(Foto 8)
Las maniobras se realizaron con extremo cuidado y conocimiento de la anatomía ya que las lesiones de los nervios sensitivos del plexo lumbar como el genitofemoral, al ser tan finos, 2mm promedio (19), son definitivas. Dicha lesión implica la aparición de anestesia en la dermatómera correspondiente.
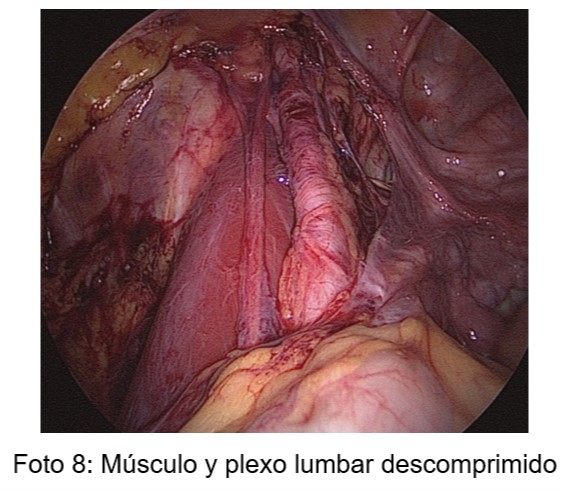
El acceso y liberación de los ligamentos redondos se efectuó por desperitonizacion paralela al recorrido del ligamento, desde su nacimiento en el útero hasta su entrada en el canal inguinal (Fotos 9 y 10).
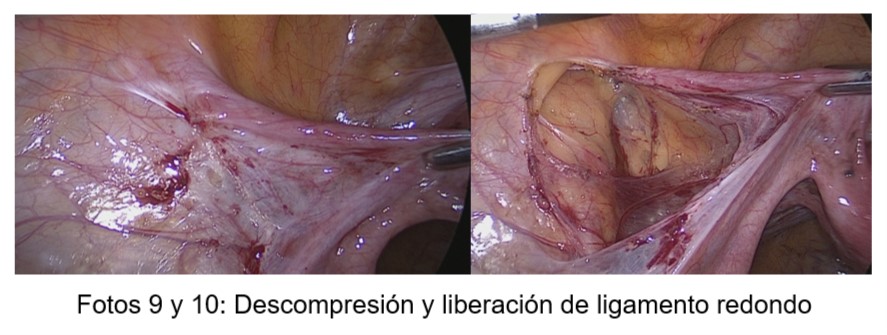
Cuando fue necesaria la descompresión y/o sección de los ligamentos uterosacros, se realizó previamente la identificación y aislamiento ureteral y del nervio hipogástrico correspondiente (zona UHU)(Foto 11).
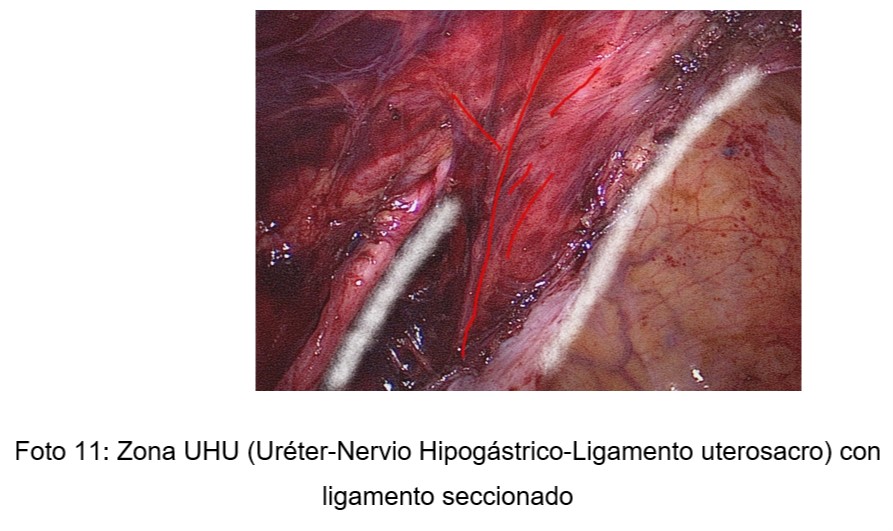
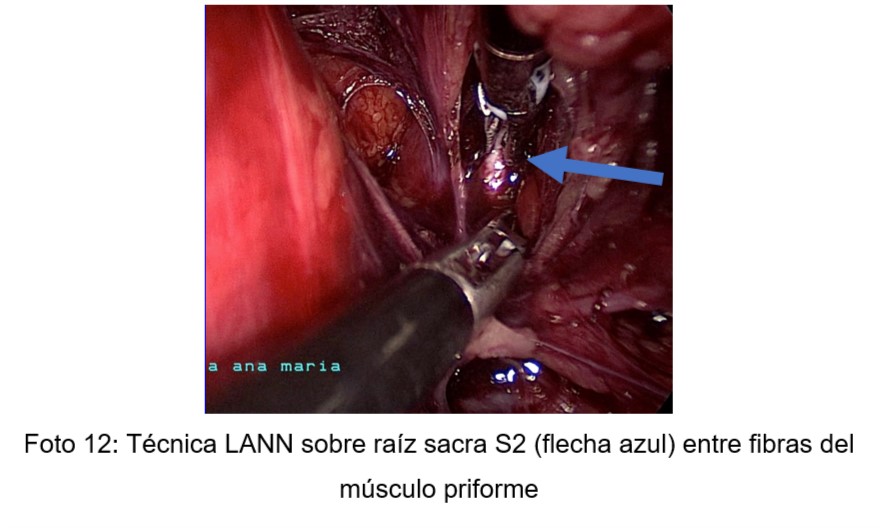
Cuando fue necesario se utilizó la técnica LANN (2) o Neuronavegación Laparoscópica que consiste en la dentificación intraoperatoria de nervios mediante estímulo a bajo voltaje con control neurofisiológico mientras se observa la respuesta motora correspondiente, según técnica descripta por Possover M. (Foto 12) (Ejemplo: estímulo de raíz sacra S2 provoca flexión de la planta del pie).
Se analizaron distintas variables prequirúrgicas, hallazgos intraoperatorios y resultados postoperatorios.
Variables prequirúrgicas
- Edad
- Paridad
- BMI (body mass index)
- ETV / RMN
- CA125
- Antecedentes quirúrgicos
- Síntomas de dolor y/o compresión (dismenorrra, dispareunia, urgencia miccional, disquecia, proctalgia, ciatalgia, dolor retrocervical, u otros)
- Score de Escala visual analógica del dolor (VAS previo)
- Presencia de sangrado uterino anormal asociado
- Esterilidad asociada
- Tiempo de evolución
Hallazgos intraoperatorias
- Hallazgo inicial
- Patología asociada
- Compromiso de los distintos nervios de plexos lumbar y sacro
- Compromiso ligamentario (redondos, uterosacros)
- Compromiso de músculo psoas-ilíaco
- Realización de Histerectomía
- Cirugía realizada
- Complicaciones intraoperatorias
- Tiempo quirúrgico
Variables postoperatorias
- Complicaciones postoperatorias
- Seguimiento-Pérdida de seguimiento
- Score de Escala visual analógica del dolor (VAS postoperatorio)
- Anatomía patológica
Se procesaron y analizaron las distintas variables con un seguimiento mínimo de 3 meses y un máximo de 18, sin pérdidas de seguimiento.
Para comparar la eficacia de la cirugía, es decir para rechazar la hipóteisis nula, se consideró el score VAS previo y el VAS postoperatorio, y se lo analizó con la prueba de los signos y la prueba de rangos signados de Wilcoxon, pruebas no paramétricas para muestras apareadas.
Con los mismos scores también se evaluó curación, mejoramiento mayor o menor al 50% y persistencia del dolor neuropático.
Resultados
Se incluyeron 28 pacientes, todas operadas por laparoscopía sin necesidad de conversión a laparotomía en ningún caso.
El edad media fue de 35 años (27-50). Respecto al status menstrual se encontró sólo una paciente menopáusica, el resto eran premenopáusicas bajo diferentes tratamientos hormonales.
Con respecto a la paridad, el 35% correspondió a pacientes nulíparas, 9% tenían un hijo y el restante 57% eran multíparas.
El body mass index arrojó un promedio de 21.32 (18,36-26,56), con la siguiente distribución:
- Bajo peso (<18.5): 7% (2p)
- Normal (18.5 – 24.9): 82% (23p)
- Sobrepeso (25 – 29.9): 11% (3p)
- Obesidad (> 30): 0
Los hallazgos ecográficos preoperatorios predominantes fueron:
- 39% Estudio normal (11p)
- 29% Endometriosis ovárica (8p)
- 18% Quiste simple (5p)
- 7% Adenomiosis (2p)
- 7% Miomatosis (2p)
Los resultados de la RMN previa con secuencia neurográfica mostraron:
- Estudio normal (8p)
- EDT ovárica (8p)
- Adenomiosis: (2p)
- Nódulo Rectovaginal: (5p)
- Adherencias utero-rectosigma: (3p)
- Nódulo Uterosacro: (2p)
- Compromiso Intestinal: (2p)
- Hidrosalpinx/hematosalpinx: (2p)
- Engrosamiento redondos: (2p)
- Engrosamiento N. Pudendo: (2p)
- Miomatosis uterina (2p)
- Dilatacion ureteral: (1p)
Los valores de CA125 oscilaron entre los 10 y 89 mU/ml con una media de 23.4 mU/ml.
El 32% de las pacientes no presentaban ningún antecedente quirúrgico, el restante 68% al menos una intervención ginecológica-obstétrica y/o abdominal:
- Endometriosis (7p)
- 4 Laparoscopías
- 3 Laparotomías
- Laparoscopías por dolor pelviano crónico (3p)
- Histeroscopía (1p)
- Miomectomia: (2p)
- Histerectomía laparotómica : (1p)
- Salpinguectomia (2p)
- ByPass Gástrico (1p)
- Apendicectomía (3p)
- Colecistectomía (2p)
- Cesáreas (4p)
- Radiofrecuencia sacral (1p)
Respecto a otros antecedentes clínicos se encontraron casos únicos de: ataque de pánico, Enfermedad Celíaca con gastritis erosiva, Tuberculosis, Diabetes, Hipotiroidismo, FIV fallida, probable fístula recto-uterina e Infarto de vena renal.
La mediana del tiempo de evolución del dolor pelviano fue de 5 años, con un mínimo de 2 y un máximo de 13 años.
La dismenorrea, la dispareunia y el dolor retrocervical fueron los síntomas más frecuentes, y se presentaron en el 81%, 85% y 90% de los pacientes respectivamente. La distribución de los síntomas fue la siguiente:
- 90% Dolor retrocervical
- 85% Dispareunia
- 81% Dismenorrea
- 33% Disquecia/proctalgia
- 28% Ciatalgia
- 28% Sangrado uterino anormal
- 14% Urgencia miccional
- 7% Esterilidad
En relación a la ubicación del dolor, sólo una paciente presentó un dolor en una única región (neuralgia del pudendo pura), el resto presentaron más de una zona de dolor: hipogastrio, fosas ilíacas, flancos, pubis, región de L1-L2, región de L2-L3, raíz de miembros inferiores, región dorso-lumbar, cúpula vaginal y región de psoas ilíaco.
El examen neuropelveológico colaboró en la identificación de zonas de dolor con sospecha de compromiso somático y/o visceral:
- 28% Dolor cérvix posterior
- 14% Ciatalgia
- 11% Región L1-L2
- 11% Región L2-L3
- 11% Región S2-S3, un caso con probable atrapamiento por músculo piriforme
- 23% Músculo psoas-ilíaco
- 5% Cicatriz de cesárea
- 5% Ligamento redondo
- 5% Engrosamiento bilateral de ligamentos uterosacros
- 11% Bloqueo pelviano completo, un caso con compromiso de plexo lumbar, ciático y pudendo izquierdos.
- 5% Debilidad muscular en ambas piernas con compresión sacral, ciática, y psoas derechos
- 5% Perdida de sensibilidad en Miembro inferior
- 5% Dolor en región de pudendo
- 5% Dolor en cúpula vaginal y región de psoas ilíaco izquierdo.
El score de VAS previo fue > 8 en el 100% de los casos correspondiendo a dolor severo.
El tiempo quirúrgico promedio fue de 123 minutos, con un mínimo de 70 y un máximo de 300 minutos.
Los hallazgos laparoscópicos iniciales más frecuentes fueron: 43% Endometriosis ovárica, 35% fibrosis, 28% bloqueo pelviano y 19% nódulo uterosacro. Las patologías asociadas encontrada fueron: adenomiosis (2p), miomatosis uterina (2p) y tumor borderline (1p).
El compromiso nervioso encontrado, considerando que una paciente puede tener varios segmentos afectados, fue: 62% nervio genitofemoral, 52% resto de plexo lumbar sensitivo, 38% hipogástrico, 33% ciático, 28% obturador, 19% pudendo y 14% raíces sacras. No se observó compromiso del nervio femoral.
Los resultados de la afección muscular-ligamentaria mostraron que el 62% (17/28) de las pacientes tenía compromiso del músculo psoas ilíaco, 54% sólo del lado derecho, 23% del izquierdo y 23% bilateral. El mismo porcentaje (62%) tenía compromiso de los ligamento redondos: 38.5% derecho, 38.5% izquierdo y 23% bilateral. Mientras que el 48% de las pacientes tenía afección con tracción sintomática de los ligamentos uterosacros, siendo el mismo 40% bilateral, 30% derecho y 30% izquierdo.
Las causas más frecuentes de atrapamiento fueron: 75% fibrosis (21p), 42% endometriosis (12p), 32% atrapamiento vascular (9p) y 3,5% tracción del ligamento del múscuo psoas-ilíaco (1p)
De las 9 pacientes con afectación del nervio ciático, 2 tenían anomalías de posición y dilatación de la vena glútea superior, 2 atrapamientos vasculares de malformaciones de ramas de la vena ilíaca y 5 atrapamientos por fibrosis.
En todas las pacientes se pudo realizar el acceso al nervio y/o ligamento y/o músculo buscado y su posterior descompresión (Fotos 13 y 14).
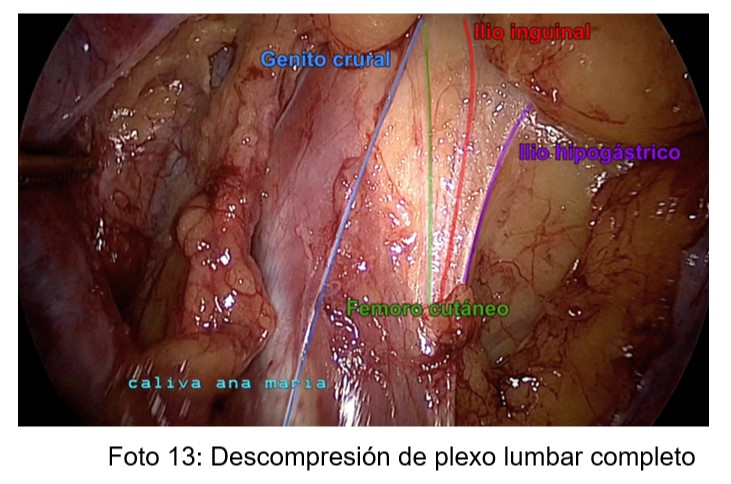
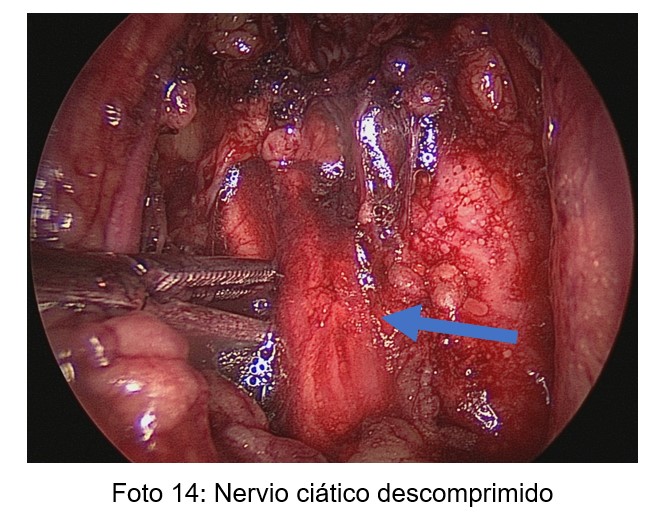
Se realizaron los siguientes procedimientos quirúrgicos asociados: descompresión de nervio hipogástrico (10p), histerectomía total laparoscópica (6p), salpinguectomía (5p), sección de ligamentos uterosacros (5p), ureterolisis (5p), anexectomía bilateral (2p), miomectomía (2p), excéresis de granuloma de cúpula (1p), sección del tendón del psoas (1p).
En 6 pacientes se complementó la cirugía con la colocación de un dispositivo intrauterino liberador de levonorgestrel (Mirenaâ) y una paciente ya lo tenía colocado (total 7 pacientes).
Se observó una sóla complicación intraoperatoria (3.5%) que consistió en un hematoma en la bifurcación aórtica que se resolvió con apertura peritoneal, drenaje y lavado de la zona, pero no estuvo relacionada con la técnica de descompresión sino con la entrada con aguja de Veress a la cavidad abdominal en una paciente extremadamente flaca (BMI 18.36)
Respecto a las complicaciones postoperatorias, se presentaron tres (10.7%): una reinternación por dolor y distensión abdominal que resolvió con analgesia y dieta; un hematoma umbilical profundo en la zona de entrada del trócar de 10mm en una paciente con antecedente de cirugía bariátrica con gran descenso de peso y sin cirugía plástica posterior de los colgajos lo que dificultó el ingreso a la cavidad; y un absceso pelviano presacral, luego de una descompresión compleja de plexo sacral que fue el único caso que necesitó de una reoperación (3.5%) para drenaje del absceso, lavado y posterior antibioticoterapia.
Por último debemos analizar el resultado principal que es la comparación entre la escala VAS previa y posterior a la intervención quirúrgica. El VAS previo promedio fue > 8 correspondiendo en todos los casos a dolor severo, mientras que el VAS posterior promedio fue de 3,25, siendo esta diferencia estadísticamente significativa tanto en la prueba de signos como en la prueba de rangos signados de Wilcoxon (valor –p< 0,0001), con el siguiente análisis:
|
Prueba de signos / Prueba bilateral: |
|
|
N+ |
27 |
|
Valore esperado |
13,500 |
|
Varianza (N+) |
6,750 |
|
valor-p (bilateral) |
< 0,0001 |
|
alfa |
0,05 |
El valor-p se calcula utilizando un método exacto.
|
Rangos con signo (Wilcoxon) / Prueba bilateral: |
|
|
V |
378 |
|
V (estandarizado) |
4,569 |
|
Valore esperado |
189,000 |
|
Varianza (V) |
1711,250 |
|
valor-p (bilateral) |
< 0,0001 |
|
alfa |
0,05 |
El valor-p exacto no ha podido calcularse. Se ha utilizado una aproximación para calcular el valor-p.
En ambas pruebas el valor –p computado es menor que el nivel de significación alfa=0.05 por lo cual se debe rechazar la hipótesis nula (H0) y aceptar la hipótesis alternativa (H1): la cirugía de descompresión neuro-vascular somática y muscular es eficaz para el tratamiento quirúrgico del dolor neuropático y lo mejora de manera estadísticamente significativa.
Todas las pacientes mejoraron luego de la cirugía: con un 64.3% de dolor leve, 32.1% de dolor moderado y sólo un 3.6%, 1 caso, de dolor severo (TABLA 1) pero con un valor menor.
TABLA 1: Comparación de VAS previo y postoperatorio de acuerdo a severidad del dolor
|
TIPO DE DOLOR |
VAS PREVIO |
VAS POSOPERAT. |
|
LEVE £3 |
0 |
64.3% (18) |
|
MODERADO 4-7 |
0 |
32.1% (9) |
|
SEVERO > 8 |
100% (28) |
3.6% (1) |
De acuerdo a los criterios de curación, mejoramiento o sin cambios, se observó:
- 30% Curación (VAS 0-1)(-p 0.016)
- 65% Mejora
- 45% Mejora VAS > 50% (9.5 a 2.6)(-p signos 0.0004 y –p Wilcoxon 0.002)
- 20% Mejora VAS < 50% (8.75 a 5.75)(-p signos 0.063 y –p Wilcoxon 0.041)
- 5% Sin cambios (VAS 10 a 8)
El 75% de las pacientes mejoraron con al menos un VAS > 50%, considerando dentro de ese grupo un 30% de curación. Mientras que si incluimos también aquellas con mejoras de VAS < 50%, el beneficio alcanza al 95% de las pacientes.
Discusión
La cirugía de descompresión neuro-vascular somática, muscular y/o ligamentaria por dolor pelviano neuropático severo puede realizarse por vía laparoscópica, con una baja tasa de complicaciones intraoperatorioas (3.5%) y postoperatorias (10.7%), sin necesidad de conversión a laparotomía. Sin embargo, es mandatorio el entrenamiento y la acreditación en cirugía laparoscópica de alta complejidad y la disponibilidad de cámaras de alta definición HD y sistemas avanzados de control de hemostasia, corte y coagulación.
El dolor pelviano neuropático se presenta con mayor frecuencia en pacientes premenopáusicas, con un promedio de edad de 35 años, probablemente relacionado con la mayor actividad hormonal con mayor grado de inflamación, congestión pelviana y tratamientos hormonales. Se observó su presencia sólo en una paciente postmenopáusica.
No parece haber diferencias respecto al antecedente de paridad y habitulamente son pacientes con un BMI normal (82%)
El examen clínico neuropelveológico fue el aporte más importante identificando en su totalidad las posibles zonas afectadas. La ecografía transvaginal identifica quistes, miomas y /o adenomiosis pero tiene casi un 40% de estudios normales, ya que pierde sensibilidad en nódulos y engrosamientos. La RMN con neurografía colabora en la identificación de dichas zonas y sobretodo en la presencia de endometriosis profunda sin embargo mostró un 28% de estudios normales probablemente por la dificultad para evaluar nervios milimétricos y zonas de fibrosis que no generen nódulos, además de depender del entrenamiento del operador en este tipo de pacientes.
El CA125 mostró una media de 23.4mU/ml lo que sugiere valores compatibles con la presencia de endometriosis pero no determinan un patrón significativo en dolor neuropático.
El 68% de las pacientes tenían algún antecedente de cirugías gineco-obstétricas y abdominales que pueden favorecer lesiones traumáticas neuropáticas y/o generación de fibrosis posquirúrgica. En las pacientes con antecedente de endometriosis, lo más frecuente es la cirugía anterior incompleta con persistencia del dolor. Así es como los hallazgos laparoscópicos iniciales más frecuentes fueron la endometriosis ovárica (43%), la fibrosis (35%), y el bloqueo pelviano completo (28%).
El dolor pelviano neuropático se caracteriza fundamentalmente por la presencia de cirugías y tratamientos médicos fallidos, con pacientes que durante años buscan soluciones, cambiando de profesionales de distintas especialidades para tratar su dolor, con un mediana del tiempo de evolución de 5 años, con un máximo que alcanzaba los 13 años.
La presencia y distribución de los síntomas es variada: la dismenorrea (81%), la dispareunia (85%) y el dolor retrocervical (90%) fueron los síntomas más frecuentes. Y el 96% de los pacientes presentaron más de una zona de dolor, lo que explica la afección de varios nervios a la vez, y confirma su origen multifactorial que aumenta la complejidad de la solución. El nervio genito-femoral (62%) y el resto del plexo lumbar sensitivo (52%) fueron los nervios más afectados, y no se encontró en ningún caso compromiso del nervio femoral.
El compromiso muscular-ligamentario también fue alto y esto determina habitualmente zonas importantes de dolor por limitación en los movimientos y actividades diarias, 62% (17/28) músculo psoas ilíaco, 62% (17/28) ligamentos redondos y 48% (13/28) ligamentos uterosacros.
El tiempo quirúrgico promedio (123min) no excede la duración de otros procedimientos de alta complejidad, aunque se trata de cirugías que exigen una extrema concentración por trabajar la mayoría del tiempo en espacios pequeños, con poco margen de maniobra y movilidad y con estructuras nobles siempre cercanas.
La fibrosis (75%) es la causa más frecuente de atrapamiento nervioso, seguido por la endometriosis (42%) y el atrapamiento vascular (32%).
En todas las pacientes se pudo realizar el acceso al nervio y/o ligamento y/o músculo buscado y su posterior descompresión con resultados favorables: de un VAS previo promedio > 8 a un VAS postoperatorio promedio de 3.25 con diferencias estadísticamentes significativas en el análisis estadístico según la prueba de signos y la prueba de rangos signados de Wilcoxon ((valor –p< 0,0001). Todas las pacientes mejoraron luego de la cirugía: con un 30% de curación y un 65% de mejoramiento: 45% con mejora del VAS > 50% de 9.5 a 2.6 (-p signos 0.0004 y –p Wilcoxon 0.002) y 25% con mejora del VAS < 50% de 8.75 a 5.75 (-p signos 0.063 y –p wilcoxon 0.041). Sólo una paciente se mantuvo dentro del VAS de dolor neuropático, con una modificación de 10 a 8.
Por lo cual se infiere que el 75% de las pacientes evolucionaron a la curación o mejoraron con un VAS > 50%; y si incluimos todas las pacientes con resultados positivos, es decir también aquellas con mejoras de VAS < 50%, el beneficio en sus distintos grados alcanza al 95%.
Dichos resultados coinciden con los reportes de Lemos N y col. que informaron un 34% de curación, un 52% de mejora con un VAS > 50%, un 12% sin cambios y un 2% de empeoramiento; con un VAS previo promedio de 8.7 y VAS postoperatorio de 2.2 (-p<0.0001), en una población de 39 años promedio de edad, con una evolución de dolor de 4 años y una media de seguimiento de 13.3 meses.
Conclusiones
La cirugía de descompresión neuro-vascular somática, muscular y/o ligamentaria realizada por laparoscopía es eficaz para el tratamiento quirúrgico del dolor neuropático en pacientes con tratamientos médicos fallidos, con una mejoría evaluada por la escala visual analógica del dolor estadísticamente significativa. El examen neuropelveológico es la clave para un correcto diagnóstico prequirúrgico y debe realizarse la descompresión de cada uno de los segmentos afectados aplicando una técnica sistemática de acceso, para no generar un daño nervioso irreversible o la aparición de nuevos dolores neuropáticos.
Debido a la causa multifactorial del dolor deberá a futuro evaluarse el efecto de la misma en trabajos prospectivos aleatorizados; no obstante la diferencia significativa encontrada entre el VAS previo y postoperatorio, y los porcentajes de curación y de mejoramiento, que globalmente alcanzan un 95%, la convierten en una opción válida.
Bibliografía
- Possover M, Forman A, Rabischong B, Lemos N, Chiantera V. Neuropelveology: New Groundbreaking Discipline in Medicine. J Minim Invasive Gynecol. 2015 Nov-Dec;22(7):1140-1.
- Possover, Rhiem, Chiantera. The "Laparoscopic Neuro-Navigation" -- LANN: from a functional cartography of the pelvic autonomous neurosystem to a new field of laparoscopic surgery. Minim Invasive Ther Allied Technol. 2004 Dec;13(5):362-7.
- Possover M. The LION procedure to the pelvic nerves for treatment of urinary and faecal disorders. Surg Technol Int. 2014 Mar;24:225-30
- Possover M, Schurch B, Henle KP. New strategies of pelvic nerves stimulation for recovery of pelvic visceral functions and locomotion in paraplegics. Neurourol Urodyn. 2010 Nov;29(8):1433-8.
- Lemos N, Possover M. Laparoscopic approach to intrapelvic nerve entrapments. J Hip Preserv Surg. 2015 Jul;2(2):92-8.
- Amarenco G, Lanoe Y, Perrigot M, Goudal H. A new canal syndrome: compression of the pudendal nerve in Alcock's canal or perinal paralysis of cyclists. Presse Med. 1987 Mar 7;16(8):399. French.
- Amarenco G, Lanoe Y, Ghnassia RT, Goudal H, Perrigot M. Alcock's canal syndrome and perineal neuralgia. Rev Neurol (Paris). 1988;144(8-9):523-6. French.
- Possover M, Quakernack J, Chiantera V. The LANN technique to reduce postoperative functional morbidity in laparoscopic radical pelvic surgery. J Am Coll Surg. 2005 Dec;201(6):913-7.
- Kavallaris A, Banz C, Chalvatzas N, Hornemann A, Luedders D, Diedrich K, Bohlman M. Laparoscopic nerve-sparing surgery of deep infiltrating endometriosis: description of the technique and patient´s outcome. Gynecology Oncology 2010.
- Fujii S, Takakura K, Matsumura N, Higuchi T, Yura S, Mandai M, Baba T, Yoshioka S. Anatomic identification and functional outcomes of the nerve sparing Okabayashi radical hysterectomy, 2007.
- Ceccaroni M, Clarizia R, Alboni C, Ruffo G, Bruni F, Roviglione G, Scioscia M, Peters I, De Placido G, Minelli L. Laparoscopic nerve-sparing transperitoneal approach for endometriosis infiltrating the pelvic wall and somatic nerves: anatomical considerations and surgical technique. Surg Radiol Anat, 2010.
- Possover M, Andersson KE, Forman A. Neuropelveology: An Emerging Discipline for the Management of Chronic Pelvic Pain. Int Neurourol J 2017; 21:243-246.
- Possover M, Schneider T, Henle KP. Laparoscopic therapy for endometriosis and vascular entrapment of sacral plexus. Fertil Steril. 2011 Feb;95(2):756-8.
- Possover M, Forman A. Pelvic Neuralgias by Neuro-Vascular Entrapment: Anatomical Findings in a Series of 97 Consecutive Patients Treated by Laparoscopic Nerve Decompression. Pain Physician. 2015 Nov;18(6):E1139-43.
- Possover M, Baekelandt J, Chiantera V. The Laparoscopic Implantation of Neuroprothesis (LION) Procedure to Control Intractable Abdomino-Pelvic Neuralgia. 2007 Jan;10(1):18-23.
- Labat JJ, Riant T, Robert R, Amarenco G, Lafaucher JP, Rigaud J. Diagnostic criteria for pudendal neuralgia by pudendal nerve entrapment (Nantes criteria). Neurourol Urodyn. 2008;27(4):306-10
- Jensen MP, Karoly P, Braver S. The measurement of clinical pain intensity: acomparison of six methods. Pain. 1986 Oct;27(1):117-26.
- Kremer E, Atkinson JH, Ignelzi RJ. Measurement of pain: patient preference does not confound pain measurement. Pain. 1981 Apr;10(2):241-8.
- Maldonado PA, Slocum PD, Chin K, Corton MM. Anatomic relationships of psoas muscle: clinical applications to psoas hitch ureteral reimplantation. Am J Obstet Gynecol. 2014 Nov;211(5):563.e1-6. doi: 10.1016/j.ajog.2014.07.008. Epub 2014 Jul 11. PubMed PMID: 25019482.
- Lemos N, Moretti Marques R, Sparapani F, Ploeger-Schor C. Nerve Entrapments, A neglected cause of perineal pain and urinary symptoms. Neurology and Urodynamics, 2015.

